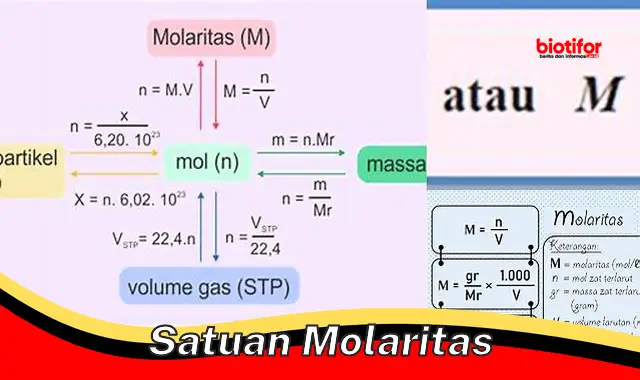
Satuan molaritas adalah satuan konsentrasi yang menyatakan jumlah mol zat terlarut per liter larutan. Satuan ini banyak digunakan dalam kimia untuk menyatakan konsentrasi larutan, terutama dalam reaksi kimia dan analisis kimia.
Satuan molaritas sangat penting karena memungkinkan kita untuk mengetahui jumlah zat terlarut yang terkandung dalam suatu larutan. Informasi ini sangat penting untuk berbagai aplikasi, seperti menentukan laju reaksi kimia, menghitung massa molar zat terlarut, dan mengontrol konsentrasi zat terlarut dalam larutan.
Dalam kimia, satuan molaritas disingkat dengan M. Misalnya, larutan dengan konsentrasi 1 M berarti mengandung 1 mol zat terlarut per liter larutan. Satuan molaritas telah digunakan sejak abad ke-19 dan masih menjadi satuan konsentrasi yang paling umum digunakan dalam kimia hingga saat ini.
satuan molaritas
Satuan molaritas adalah satuan konsentrasi yang penting dalam kimia. Satuan ini memiliki beberapa aspek penting, yaitu:
- Definisi: Jumlah mol zat terlarut per liter larutan
- Satuan: Molar (M)
- Penggunaan: Menyatakan konsentrasi larutan
- Aplikasi: Reaksi kimia, analisis kimia
- Sejarah: Digunakan sejak abad ke-19
- Manfaat: Memudahkan perhitungan kimia
- Keterkaitan: Dengan konsentrasi lain (molalitas, persen)
- Contoh: Larutan 1 M mengandung 1 mol zat terlarut per liter larutan
Satuan molaritas sangat penting dalam kimia karena memungkinkan kita untuk mengetahui jumlah zat terlarut dalam suatu larutan. Informasi ini sangat penting untuk berbagai aplikasi, seperti menentukan laju reaksi kimia, menghitung massa molar zat terlarut, dan mengontrol konsentrasi zat terlarut dalam larutan.
Definisi
Definisi satuan molaritas adalah jumlah mol zat terlarut per liter larutan. Definisi ini penting karena menjelaskan secara tepat apa yang dimaksud dengan satuan molaritas dan bagaimana cara menghitungnya. Definisi ini juga menjadi dasar untuk semua aplikasi satuan molaritas dalam kimia.
Definisi satuan molaritas juga penting karena menunjukkan hubungan antara satuan molaritas dan konsep konsentrasi larutan. Konsentrasi larutan adalah ukuran jumlah zat terlarut dalam larutan. Satuan molaritas adalah salah satu cara untuk menyatakan konsentrasi larutan, dan definisinya menunjukkan bahwa satuan molaritas berbanding lurus dengan konsentrasi larutan.
Sebagai contoh, larutan dengan konsentrasi 1 M mengandung 1 mol zat terlarut per liter larutan. Ini berarti bahwa dalam 1 liter larutan tersebut, terdapat 1 mol zat terlarut. Informasi ini sangat penting untuk berbagai aplikasi kimia, seperti menentukan laju reaksi kimia dan menghitung massa molar zat terlarut.
Memahami definisi satuan molaritas sangat penting untuk dapat menggunakan satuan molaritas secara efektif dalam kimia. Definisi ini memberikan dasar untuk semua aplikasi satuan molaritas dan memungkinkan kita untuk menghitung dan menggunakan satuan molaritas dengan benar.
Satuan
Satuan molaritas, yang dinyatakan dalam molar (M), adalah satuan konsentrasi yang banyak digunakan dalam kimia. Satuan ini menunjukkan jumlah mol zat terlarut per liter larutan. Pemahaman tentang hubungan antara satuan molar dan satuan molaritas sangat penting untuk menggunakan satuan molaritas secara efektif dalam berbagai aplikasi kimia.
-
Definisi Satuan Molar
Satuan molar adalah satuan jumlah zat yang didefinisikan sebagai jumlah zat yang mengandung 6,022140761023 entitas elementer. Entitas elementer dapat berupa atom, molekul, ion, atau elektron.
-
Penggunaan Satuan Molar dalam Satuan Molaritas
Dalam satuan molaritas, satuan molar digunakan sebagai penyebut untuk menyatakan jumlah mol zat terlarut per liter larutan. Satuan liter (L) digunakan sebagai penyebut untuk menyatakan volume larutan.
-
Konversi Satuan Molaritas
Satuan molaritas dapat dikonversi ke satuan konsentrasi lainnya, seperti molalitas (m) dan persen (%). Konversi ini penting untuk dapat menggunakan satuan molaritas dalam berbagai aplikasi kimia.
-
Aplikasi Satuan Molaritas
Satuan molaritas banyak digunakan dalam berbagai aplikasi kimia, seperti penentuan laju reaksi, perhitungan massa molar, dan pengendalian konsentrasi zat terlarut dalam larutan.
Dengan memahami hubungan antara satuan molar dan satuan molaritas, kita dapat menggunakan satuan molaritas secara efektif dalam berbagai aplikasi kimia. Satuan molaritas memungkinkan kita untuk menyatakan konsentrasi larutan secara jelas dan akurat, sehingga memudahkan kita untuk melakukan perhitungan dan analisis kimia.
Penggunaan
Satuan molaritas sangat penting dalam kimia karena memungkinkan kita untuk menyatakan konsentrasi larutan. Konsentrasi larutan adalah ukuran jumlah zat terlarut dalam larutan, dan satuan molaritas memberikan cara yang jelas dan akurat untuk menyatakan konsentrasi ini.
-
Penentuan Laju Reaksi
Satuan molaritas digunakan untuk menentukan laju reaksi kimia. Laju reaksi adalah ukuran seberapa cepat suatu reaksi kimia berlangsung, dan satuan molaritas digunakan untuk menyatakan konsentrasi reaktan dan produk dalam reaksi.
-
Perhitungan Massa Molar
Satuan molaritas juga digunakan untuk menghitung massa molar zat terlarut. Massa molar adalah massa satu mol suatu zat, dan satuan molaritas digunakan untuk menentukan jumlah mol zat terlarut dalam suatu larutan.
-
Pengendalian Konsentrasi Zat Terlarut
Satuan molaritas digunakan untuk mengontrol konsentrasi zat terlarut dalam larutan. Konsentrasi zat terlarut harus dikontrol dalam banyak aplikasi, seperti dalam produksi obat-obatan dan bahan kimia.
-
Analisis Kimia
Satuan molaritas digunakan dalam berbagai teknik analisis kimia, seperti titrasi dan spektrofotometri. Teknik-teknik ini digunakan untuk menentukan konsentrasi zat terlarut dalam larutan.
Dengan demikian, satuan molaritas adalah satuan yang sangat penting dalam kimia karena memungkinkan kita untuk menyatakan konsentrasi larutan secara jelas dan akurat. Satuan molaritas digunakan dalam berbagai aplikasi, mulai dari penentuan laju reaksi hingga analisis kimia.
Aplikasi
Satuan molaritas sangat penting dalam reaksi kimia dan analisis kimia karena memungkinkan kita untuk mengetahui konsentrasi reaktan dan produk. Konsentrasi reaktan dan produk sangat penting untuk menentukan laju reaksi dan hasil reaksi. Dalam analisis kimia, satuan molaritas digunakan untuk menentukan konsentrasi zat terlarut dalam suatu larutan. Konsentrasi zat terlarut sangat penting untuk menentukan identitas dan kuantitas zat terlarut tersebut.
Sebagai contoh, dalam reaksi kimia antara asam klorida (HCl) dan natrium hidroksida (NaOH), satuan molaritas digunakan untuk menentukan konsentrasi asam klorida dan natrium hidroksida. Konsentrasi asam klorida dan natrium hidroksida akan menentukan laju reaksi dan hasil reaksi. Dalam analisis kimia, satuan molaritas digunakan untuk menentukan konsentrasi suatu zat terlarut dalam suatu larutan. Misalnya, dalam analisis kadar gula dalam darah, satuan molaritas digunakan untuk menentukan konsentrasi gula dalam darah.
Dengan demikian, satuan molaritas sangat penting dalam reaksi kimia dan analisis kimia karena memungkinkan kita untuk mengetahui konsentrasi reaktan, produk, dan zat terlarut. Konsentrasi ini sangat penting untuk menentukan laju reaksi, hasil reaksi, dan identitas serta kuantitas zat terlarut.
Sejarah
Penggunaan satuan molaritas dalam kimia telah melalui perjalanan panjang sejak pertama kali diperkenalkan pada abad ke-19. Sejak saat itu, satuan molaritas telah menjadi satuan konsentrasi yang banyak digunakan dan sangat penting dalam berbagai bidang kimia.
-
Perkembangan Awal
Konsep konsentrasi larutan telah dikenal sejak zaman kuno, namun baru pada abad ke-19 satuan molaritas diperkenalkan secara formal. Pada awalnya, satuan molaritas digunakan untuk menyatakan konsentrasi asam dan basa, namun kemudian penggunaannya diperluas ke berbagai jenis larutan.
-
Peranan Penting dalam Kimia
Penggunaan satuan molaritas sangat penting dalam kimia karena memungkinkan para ilmuwan untuk membandingkan konsentrasi larutan yang berbeda dan untuk memprediksi perilaku kimia dari larutan tersebut. Satuan molaritas juga memudahkan perhitungan kuantitatif dalam reaksi kimia dan analisis kimia.
-
Penggunaan Luas di Berbagai Bidang
Saat ini, satuan molaritas digunakan secara luas di berbagai bidang kimia, termasuk kimia analitik, kimia organik, dan kimia fisik. Satuan molaritas juga banyak digunakan dalam industri, seperti industri makanan, minuman, dan farmasi.
-
Standarisasi Internasional
Satuan molaritas telah distandarisasi secara internasional, sehingga dapat digunakan dan dipahami oleh para ilmuwan di seluruh dunia. Hal ini sangat penting untuk kolaborasi ilmiah dan pertukaran informasi.
Dengan demikian, sejarah penggunaan satuan molaritas sejak abad ke-19 menunjukkan pentingnya satuan konsentrasi ini dalam perkembangan kimia. Satuan molaritas terus menjadi alat yang sangat penting dalam berbagai bidang kimia dan akan terus memainkan peran penting dalam kemajuan ilmu kimia di masa depan.
Manfaat
Satuan molaritas memudahkan perhitungan kimia dengan menyediakan cara yang jelas dan sistematis untuk menyatakan konsentrasi larutan. Satuan molaritas memungkinkan kita untuk menghitung jumlah zat terlarut, volume larutan, dan konsentrasi larutan dengan mudah dan akurat.
-
Penentuan Jumlah Zat Terlarut
Satuan molaritas dapat digunakan untuk menentukan jumlah zat terlarut dalam suatu larutan. Jumlah zat terlarut dinyatakan dalam mol, dan dapat dihitung dengan mengalikan konsentrasi larutan (dalam M) dengan volume larutan (dalam L). Informasi ini sangat penting untuk berbagai aplikasi, seperti menentukan laju reaksi dan menghitung massa molar zat terlarut.
-
Penentuan Volume Larutan
Satuan molaritas juga dapat digunakan untuk menentukan volume larutan yang diperlukan untuk menyiapkan larutan dengan konsentrasi tertentu. Volume larutan dapat dihitung dengan membagi jumlah zat terlarut (dalam mol) dengan konsentrasi larutan (dalam M). Informasi ini sangat penting untuk menyiapkan larutan dengan konsentrasi yang tepat untuk berbagai aplikasi.
-
Pengenceran Larutan
Satuan molaritas sangat berguna untuk mengencerkan larutan. Pengenceran larutan melibatkan penambahan pelarut ke larutan untuk mengurangi konsentrasinya. Satuan molaritas dapat digunakan untuk menghitung volume pelarut yang diperlukan untuk mengencerkan larutan ke konsentrasi yang diinginkan.
-
Reaksi Kimia Stoikiometri
Satuan molaritas memainkan peran penting dalam reaksi kimia stoikiometri. Reaksi kimia stoikiometri adalah reaksi kimia yang terjadi dalam perbandingan mol tertentu. Satuan molaritas dapat digunakan untuk menentukan jumlah reaktan dan produk yang terlibat dalam suatu reaksi kimia stoikiometri.
Dengan demikian, satuan molaritas sangat bermanfaat untuk memudahkan perhitungan kimia. Satuan molaritas menyediakan cara yang jelas dan sistematis untuk menyatakan konsentrasi larutan, yang memungkinkan kita untuk menghitung jumlah zat terlarut, volume larutan, dan konsentrasi larutan dengan mudah dan akurat.
Keterkaitan
Satuan molaritas memiliki keterkaitan dengan konsentrasi lain, seperti molalitas (m) dan persen (%). Keterkaitan ini penting untuk dipahami karena memungkinkan kita untuk mengonversi satuan molaritas ke satuan konsentrasi lain, sehingga memudahkan kita untuk menggunakan satuan konsentrasi yang sesuai untuk aplikasi tertentu.
Konversi antara satuan molaritas dan molalitas memperhitungkan massa jenis pelarut, sedangkan konversi antara satuan molaritas dan persen memperhitungkan massa jenis larutan. Konversi ini dapat dilakukan dengan menggunakan rumus-rumus berikut:
- Molaritas (M) = Molalitas (m) x Massa jenis pelarut (kg/L)
- Molaritas (M) = Persen (%) x 10 / (Massa molar zat terlarut (g/mol) x Massa jenis larutan (kg/L))
Pemahaman tentang keterkaitan antara satuan molaritas dan konsentrasi lain sangat penting dalam berbagai aplikasi kimia. Misalnya, dalam analisis kimia, kita mungkin perlu mengonversi konsentrasi suatu larutan dari satuan molaritas ke satuan persen untuk membandingkannya dengan standar atau untuk menghitung massa zat terlarut yang diperlukan untuk menyiapkan larutan dengan konsentrasi tertentu.
Dengan demikian, keterkaitan antara satuan molaritas dan konsentrasi lain sangat penting untuk dipahami karena memungkinkan kita untuk mengonversi satuan molaritas ke satuan konsentrasi lain, sehingga memudahkan kita untuk menggunakan satuan konsentrasi yang sesuai untuk aplikasi tertentu.
Contoh
Contoh “Larutan 1 M mengandung 1 mol zat terlarut per liter larutan” merupakan ilustrasi penting dari konsep satuan molaritas. Satuan molaritas didefinisikan sebagai jumlah mol zat terlarut per liter larutan, dan contoh ini menunjukkan bagaimana satuan molaritas digunakan untuk menyatakan konsentrasi larutan.
Dalam contoh tersebut, larutan 1 M mengandung 1 mol zat terlarut per liter larutan. Artinya, dalam setiap liter larutan tersebut, terdapat 1 mol zat terlarut. Informasi ini sangat penting karena memungkinkan kita untuk mengetahui jumlah zat terlarut yang terkandung dalam larutan, yang selanjutnya dapat digunakan untuk berbagai aplikasi, seperti menentukan laju reaksi kimia, menghitung massa molar zat terlarut, dan mengontrol konsentrasi zat terlarut dalam larutan.
Memahami hubungan antara contoh ini dan satuan molaritas sangat penting karena memungkinkan kita untuk menggunakan satuan molaritas secara efektif dalam kimia. Satuan molaritas adalah satuan konsentrasi yang penting, dan contoh yang diberikan memberikan gambaran jelas tentang bagaimana satuan molaritas digunakan untuk menyatakan konsentrasi larutan.
Pertanyaan Umum tentang Satuan Molaritas
Berikut adalah beberapa pertanyaan umum tentang satuan molaritas:
Pertanyaan 1: Apa yang dimaksud dengan satuan molaritas?
Satuan molaritas adalah satuan konsentrasi yang menyatakan jumlah mol zat terlarut per liter larutan.
Pertanyaan 2: Mengapa satuan molaritas penting dalam kimia?
Satuan molaritas penting dalam kimia karena memungkinkan kita untuk mengetahui jumlah zat terlarut yang terkandung dalam suatu larutan. Informasi ini sangat penting untuk berbagai aplikasi, seperti menentukan laju reaksi kimia, menghitung massa molar zat terlarut, dan mengontrol konsentrasi zat terlarut dalam larutan.
Pertanyaan 3: Bagaimana cara menghitung satuan molaritas?
Satuan molaritas dapat dihitung dengan membagi jumlah mol zat terlarut dengan volume larutan dalam liter.
Pertanyaan 4: Apa perbedaan antara molaritas dan molalitas?
Molaritas adalah jumlah mol zat terlarut per liter larutan, sedangkan molalitas adalah jumlah mol zat terlarut per kilogram pelarut.
Pertanyaan 5: Bagaimana cara mengonversi satuan molaritas ke konsentrasi lain?
Satuan molaritas dapat dikonversi ke konsentrasi lain, seperti molalitas dan persen, menggunakan rumus-rumus tertentu.
Pertanyaan 6: Apa saja aplikasi satuan molaritas dalam kehidupan sehari-hari?
Satuan molaritas memiliki berbagai aplikasi dalam kehidupan sehari-hari, seperti dalam pengendalian kualitas air, pengujian kadar gula darah, dan produksi obat-obatan.
Kesimpulan
Satuan molaritas adalah satuan konsentrasi yang penting dalam kimia. Satuan molaritas digunakan untuk menyatakan konsentrasi larutan dan memiliki berbagai aplikasi dalam penelitian, industri, dan kehidupan sehari-hari.
Artikel Terkait
Untuk mempelajari lebih lanjut tentang satuan molaritas, silakan kunjungi artikel berikut:
- Artikel 1
- Artikel 2
- Artikel 3
Tips Menggunakan Satuan Molaritas
Satuan molaritas adalah satuan konsentrasi yang penting dalam kimia. Berikut adalah beberapa tips untuk menggunakan satuan molaritas secara efektif:
Tip 1: Pahami Definisi Satuan Molaritas
Satuan molaritas adalah jumlah mol zat terlarut per liter larutan. Memahami definisi ini sangat penting untuk menggunakan satuan molaritas dengan benar.
Tip 2: Gunakan Satuan Molaritas dengan Benar
Satuan molaritas dinyatakan dalam molar (M). pastikan untuk menggunakan satuan ini dengan benar saat menyatakan konsentrasi larutan.
Tip 3: Konversi Satuan Molaritas
Satuan molaritas dapat dikonversi ke satuan konsentrasi lainnya, seperti molalitas dan persen. Ketahui cara mengonversi satuan molaritas untuk memudahkan perhitungan kimia.
Tip 4: Hitung Satuan Molaritas dengan Tepat
Satuan molaritas dihitung dengan membagi jumlah mol zat terlarut dengan volume larutan dalam liter. Pastikan untuk mengukur volume larutan dengan tepat untuk mendapatkan hasil yang akurat.
Tip 5: Terapkan Satuan Molaritas dalam Aplikasi Kimia
Satuan molaritas memiliki berbagai aplikasi dalam kimia, seperti menentukan laju reaksi, menghitung massa molar, dan mengendalikan konsentrasi zat terlarut. Pahami konsep ini untuk mengaplikasikannya secara efektif.
Dengan mengikuti tips ini, Anda dapat menggunakan satuan molaritas secara efektif dan akurat dalam aplikasi kimia.
Kesimpulan
Satuan molaritas adalah satuan konsentrasi yang penting dalam kimia. Dengan memahami definisi, penggunaan, dan aplikasi satuan molaritas, Anda dapat menggunakannya dengan efektif untuk berbagai perhitungan dan analisis kimia.
Kesimpulan Satuan Molaritas
Satuan molaritas merupakan satuan konsentrasi yang sangat penting dalam bidang kimia. Satuan ini digunakan untuk menyatakan jumlah mol zat terlarut per liter larutan. Satuan molaritas memiliki peran penting dalam berbagai aspek kimia, seperti penentuan laju reaksi, perhitungan massa molar, pengendalian konsentrasi zat terlarut, dan analisis kimia.
Memahami konsep satuan molaritas sangat penting bagi siapa saja yang ingin mendalami bidang kimia. Dengan memahami satuan molaritas, kita dapat melakukan perhitungan dan analisis kimia secara akurat dan efektif. Oleh karena itu, penguasaan satuan molaritas menjadi salah satu kunci dalam pengembangan ilmu kimia dan aplikasinya di berbagai bidang kehidupan.
Youtube Video:
